La evolución de los seres humanos siempre se ha sustentado sobre 2 pilares fundamentales, que como son la alimentación y la energía. Los macronutrientes que favorecen el desarrollo de las plantas son el Nitrógeno (N), Fosforo (P) y Potasio (K). Es por ello que, el uso de fertilizantes con base en N, ha supuesto un aumento de la producción agrícola de la tierra, gracias a proporcionar los nutrientes esenciales para potenciar su crecimiento. Consecuentemente, la Tierra ha padecido un aumento exponencial de la población humana pasando de los 2000 M de habitantes en 1930, a 8000M en 2023.
Desde el origen de los tiempos, el empleo de los excrementos de los animales como abono natural ha sido una constante, dado que era evidente el efecto potenciador que tenía en el crecimiento de las plantas. Sin embargo, fue el químico alemán Fritz Haber quien consiguió la manera de utilizar el nitrógeno del aire para desarrollar la síntesis de amoníaco (NH₃), hecho que le valió el prestigioso Premio Nobel de Química de 1918. De esa manera, se dejó de lado el uso del abono natural, para evolucionar hacia la era de los abonos artifíciales. Por el camino, Chile fue uno de los países más perjudicados, porque por aquel entonces fue quien exportaba la materia prima necesaria.
Posteriormente, fue Carl Bosch quien permitió escalar el proceso, derivando todo ello en la industrialización de la síntesis de amoniaco. Por corolario, en 1931 le fue otorgado el premio Nobel de Química, compartido con Friedrich Bergius, por el descubrimiento y desarrollo del método de síntesis química a alta presión.
El amoníaco
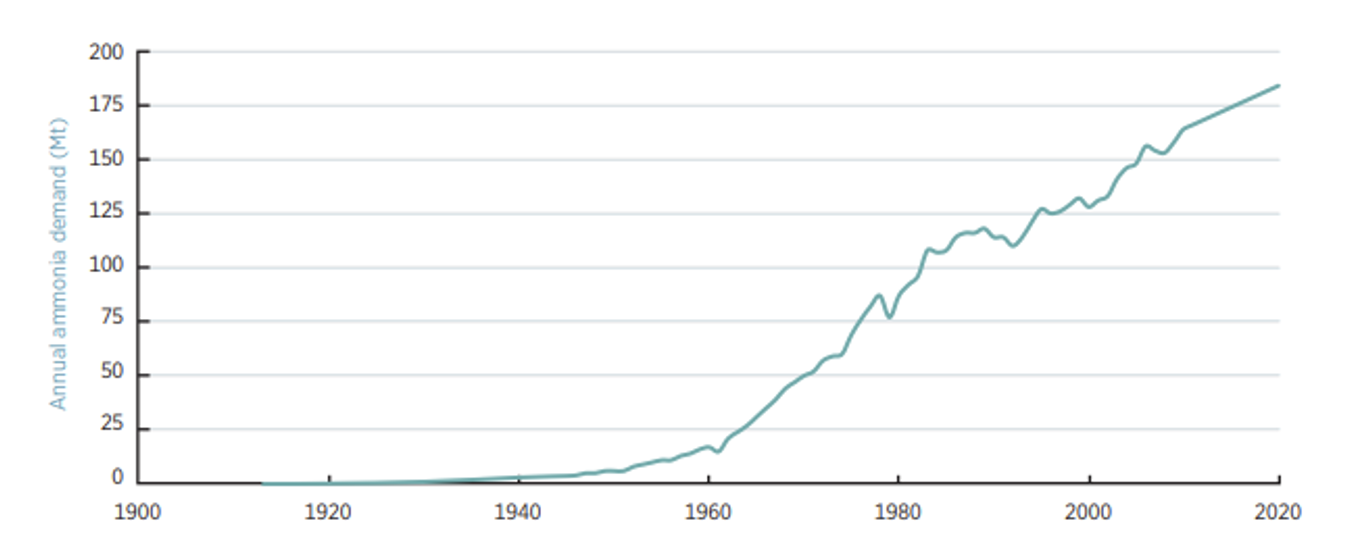
El precursor necesario que se usa para generar fertilizantes en base N es el amoníaco (NH₃), para posteriormente, obtener productos como nitrato amónico, sales amónicas y urea. En la siguiente gráfica podéis observar la evolución de la producción de amoníaco, quedando patente como tras el descubrimiento del proceso Haber-Bosch la producción anual ha aumentado de manera progresiva en los últimos 80 años.
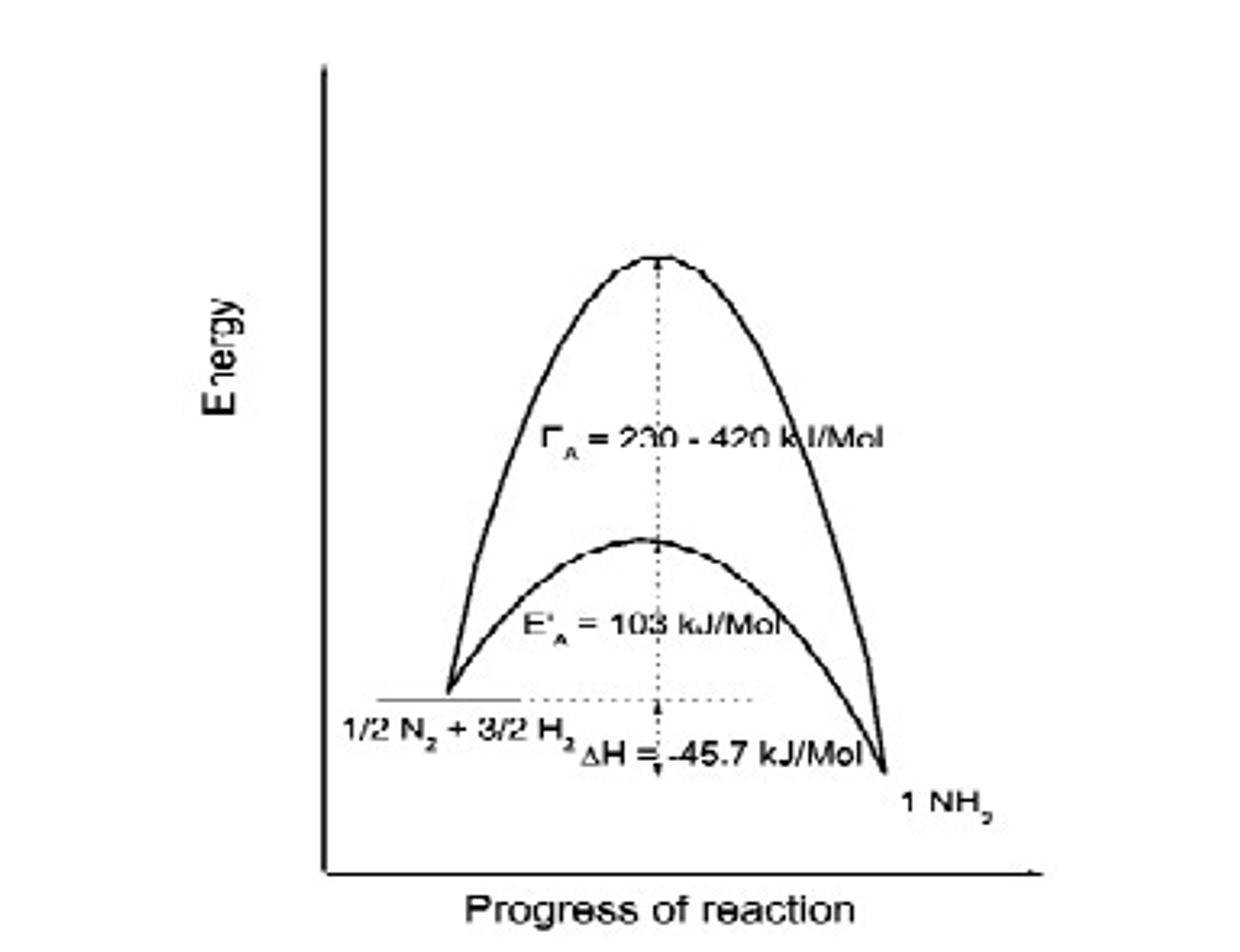
 Asier Aranzabal, profesor ingeniería química de la Universidad del País Vasco (EHU/UPV), me explicó un día que él en las clases de Universidad empleaba el símil de una carrera olímpica de vallas. La barrera cinética son las vallas. Si las vallas son demasiado altas, y nuestro pie no alcanza a superarlas. Para eso empleamos los catalizadores, que nos permiten reducir la barrera cinética. Algo así como, reducir la altura de la valla, permitiéndonos superar con más facilidad y correr más ( + velocidad = + cinética) para alcanzar las condiciones del equilibrio termodinámico que hemos descrito previamente.
Asier Aranzabal, profesor ingeniería química de la Universidad del País Vasco (EHU/UPV), me explicó un día que él en las clases de Universidad empleaba el símil de una carrera olímpica de vallas. La barrera cinética son las vallas. Si las vallas son demasiado altas, y nuestro pie no alcanza a superarlas. Para eso empleamos los catalizadores, que nos permiten reducir la barrera cinética. Algo así como, reducir la altura de la valla, permitiéndonos superar con más facilidad y correr más ( + velocidad = + cinética) para alcanzar las condiciones del equilibrio termodinámico que hemos descrito previamente.